Silicagel er det materialet i granulat som vi blant annet finner i de kjente «DO NOT EAT»-posene, ofte fast i skoesker og i emballasje generelt. Dens funksjon er like «enkel» som den er viktig: absorbere fuktighet. Nettopp på grunn av denne dehydrerende kapasiteten brukes den også i andre områder, hvor det er nødvendig å holde noe tørt, enten det er elektroniske komponenter, bøker eller faktisk klær og sko. Men hvordan «fanger» den vannet i luften så godt? Svaret ligger i hans kjemisk struktur. Silikagel er ingenting annet enn amorf silika som er arrangert i en ekte porøst nettverk. Det er som om det er en lite nettverk full av hull (porene) ordnet her og der klar for fange opp vannmolekylerlike liten. I tillegg til tilstedeværelsen av porer, takket være noen kjemiske grupper som er i stand til å binde vanndet samme gel overflate hjelper absorbere fuktighet. På denne måten er silikagelen i stand til å holde på store mengder H2Eller på overflaten uten å bli myk eller smelte. I utgangspunktet er triksene hans: massevis av porer, mye overflate og mange steder hvor vann fester seg. På denne måten klarer den å beholde opptil 40 % av vekten. Det er en enkel, stabil og effektiv mekanisme som gjør silikagel til et av de beste tekniske tørkemidlene som finnes.
Hva silikagel er og hvordan det fungerer: en gigantisk skjult overflate
Ved første øyekast ser det ut som sand, men fra et kjemisk synspunkt er silikagel det amorft silisiumdioksiden ikke-krystallinsk silikastruktur, dvs. ikke ordnet og regelmessig i rommet, men rotete og «kaotisk». Denne lidelsen er nettopp det som lar oss ha en porøs struktur som er i stand til å eliminere fuktighet fra luften; for å få det, spesielle kjemiske prosedyrer kalt «sol-gel” Disse prosessene skaper et uregelmessig tredimensjonalt nettverk med mikroporermindre enn 2 nanometer i størrelse, f.eks mesoporeneopptil 50 nanometer i størrelse. Det er nettopp dette mangfoldet av uregelmessige hulrom som gjør materialet så effektivt: et gram silikagel kan ha 700 m² innvendig overflatenesten like mye som to basketballbaner presset inn i en teskje! Er ikke det imponerende?
Denne enorme overflaten er det virkelige «hemmelige våpenet»: mer overflateareal betyr mer plass for å romme vannmolekyler. Takket være den uordnede arkitekturen til amorf silika, vann kan komme overalt og finn et punkt som holder det. Det er litt som å gå inn i et hus med tusen hyller: Jo flere hyller du har, jo flere ting kan du plassere på dem. Her er hver hylle en pore.
Hvorfor vann fester seg: kjemien til adsorpsjon
La oss nå komme til kjernen av fenomenet: adsorpsjon. Og nei, vi stavet det ikke feil: vi snakker om adsorpsjon og ikke absorpsjon (som en svamp som inneholder vann). Det er et ekte kjemisk-fysisk fenomen som vi kan definere som en slags «overflatevedheft». Enkelt sagt, når en gass når overflaten av et fast materiale, vil gassmolekylene – av H2Eller tilstede i luften som vanndamp i vårt tilfelle – de kan «hvile» på overflatelaget av materialet.
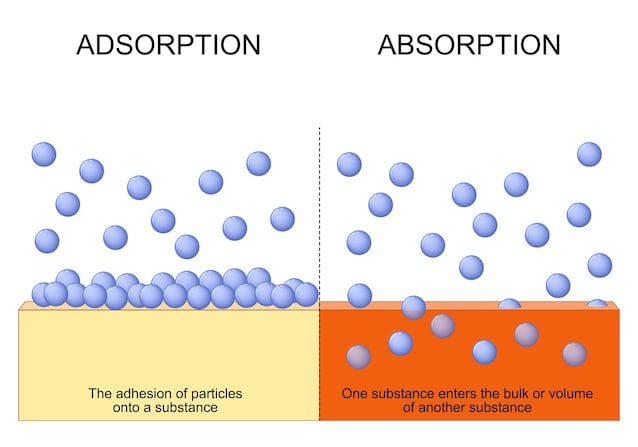
Dette fenomenet kan være mer eller mindre sterk basert på interaksjonene som dannes mellom det faste materialet og gassen det kommer i kontakt med: for eksempel kan gassformige molekyler som adsorberer uten spesielle interaksjoner med materialet lett «desorbere» og fly vekk igjen; hvis de er dannet kjemiske bindingervil det være svært vanskelig, om ikke umulig, å bryte bindingen mellom materialet og gassen.
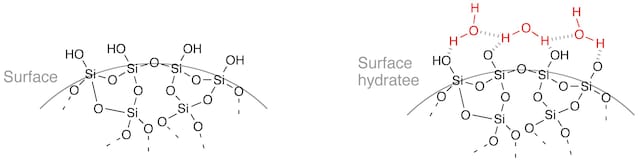
Når det gjelder silikagel, skjer adsorpsjon takket være samspillet mellom noen kjemiske grupper som er tilstede på gitteret og vannet i luften. Overflaten av gelen er faktisk full av grupper kalt «silanoler» (Si-OH), dannet av et silisiumatom og en hydroksylgruppe (OH) som har en sterk tilhørighet med H-molekyler2O. Tilstedeværelsen av disse overflategruppene tillater dannelsen av en hydrogenbinding som ikke lenger lar vannet slippe ut. Selv om de ikke er like sterke som de kovalente bindingene som skapes i en faktisk kjemisk reaksjon, er interaksjonen mellom de to gruppene fortsatt sterk nok til å fjerne fuktighet fra luften og aldri la den gå bort (med mindre eksterne faktorer som varme griper inn).
Kombinert sammen forklarer dannelsen av overflatebindinger og den høye porøse overflaten hvorfor silikagel kan holde på opptil 40 % av vekten i vannen bemerkelsesverdig prestasjon for et så enkelt og stabilt materiale.
Hva skjer videre?
Det interessante og nysgjerrige er at en gang mettet (dvs. når overflaten er fylt med vann), «setter» ikke silikagelen vann og deformeres ikke ved mykning. Det gjenstår solid, stiv og sikker selv ved full last. Dette er en av grunnene til at det er valgt for delikate produkter som medisiner, elektroniske enheter, kameralinser, tørket mat og til og med museumssamlinger.
Etter metning kan gelen enkelt regenereres varme den opp. Varmen bryter hydrogenbindingene med vannet og lar det gjøre det fordampe; en gang avkjølt, gelen kommer tilbake klar til bruk igjen nettverket av porer.
I praksis fungerer silikagel som en stille vokter mot fuktighet: den lager ikke støy, den beveger seg ikke, den endrer ikke form, men den fortsetter å fange vann i det uendelige som om han hadde en superkraft. Og alt dette takket være strukturer som er usynlige for det blotte øye, porer og bindinger som «fanger» irriterende fuktighet.
Kilder
Kjemien til silika. Løselighet, polymerisering, kolloid- og overflateegenskaper og biokjemi. Von RK Iler. John Wiley and Sons, Chichester 1979. XXIV Brinker, C.J., & Scherer, G.W. Sol-Gel Science: The Physics and Chemistry of Sol-Gel Processing. Academic Press, 1990. Overflatekjemien til amorf silika. Zhuravlev-modellen Chua, H., Ng, K. C., Chakraborty, A., Oo, N. M., & Othman, M. A. (2002). Adsorpsjonsegenskaper til silikagel + vannsystemer. Journal of Chemical and Engineering Data, 47, 1177-1181

