Metallnatrium (symbol Na) er et element i den første gruppen av det periodiske tabellen, det av Alkaliske metaller. Disse metallene har en enkelt Elektron i det eksterne skallet og pleier å Selg den enkelt: Derfor er natrium ekstremt reaktivspesielt medfosssom han produserer gjennom en eksosterisk natriumhydroksydreaksjon (NaOH), gassformig hydrogen (H2) og varme tilstrekkelig til å utløse eksplosjonen. I denne artikkelen ser vi i detalj kjemi av natrium, der det er i natur og de viktigste applikasjonene.
Den eksplosive reaksjonen på natrium med vann
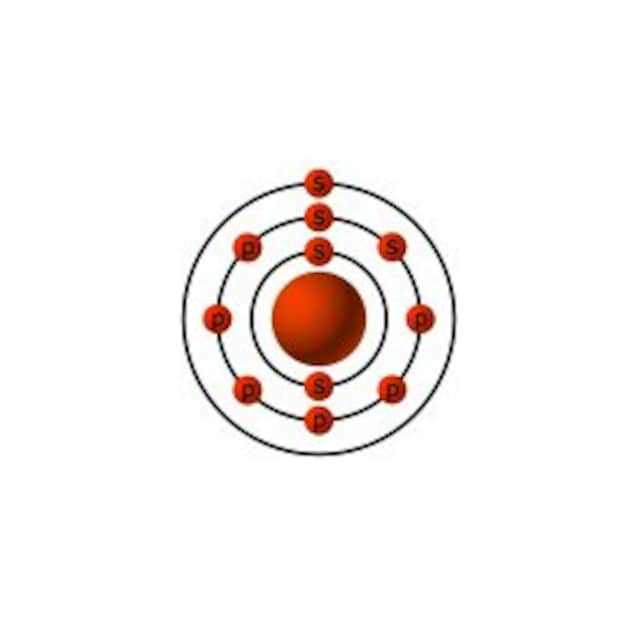
For å forstå hvorfor natrium eksploderer i kontakt med vann, må vi kjenne strukturen til natriumatom. Natriumatom presenterer 11 protoner Og 11 elektronersom er fordelt på tre nivåer: 2-8-1. Det tredje nivået elektron er lite knyttet til kjernen og kommer sedet Med letthet. Så snart natrium kommer inn i kontakt med vann, gir natriumet elektronet gjennom følgende kjemiske reaksjon.
2 Na + 2 H2Eller ⟶ 2 nah + h2 + varme
De varme utviklet lar hydrogen reagere medoksygen Til stede i luften, brenne og forårsake eksplosjonen.
2 h2 +O2⟶ 2 timer2ELLER
Der metallnatrium finnes i naturen og hvordan det oppnås
De ren natrium det er ikke funnet aldri I naturen, siden det alltid er knyttet til andre elementer. For eksempel, hvis kombinert med Klordanner natriumkloridbedre kjent som kjøkkensalt eller havsalt. Av denne grunn er kjøkkenet salt eksploderer ikke I kontakt med vann: natrium er knyttet til klor og finnes ikke i elementær form.
Det meste av natrium til stede i naturen finnes i Havi form av natriumklorid. Faktisk inneholder havene omtrent 4 × 10 kg av dette saltet, eller 40 milliarder milliarder kilo. Hvis vi samler alt dette saltet, ville vi få en gigantisk kube med en side på 265 km, så stor som avstanden som skiller Milano fra Venezia.

I alle fall kan natrium også finnes i andre mineraler, for eksempel silikater, sulfater og karbonater. Faktisk det kjemiske symbolet «Na«stammer fra» natrium «, som refererer til»Natrun«, Det arabiske navnet for hydrert natriumkarbonat, et mineral som inneholder natrium.
For å oppnå rent natrium, brukes flere kjemiske prosesser det separate natrium fra de andre elementene. En av disse er Downs -prosesshvor natriumklorid er slått sammen (dvs. væske laget). I denne væsken settes to elektroder inn og en potensiell forskjell blir brukt. Takket være dette gir natriumklorid opp et natriumelektron, som er avsatt på en av elektrodene i form av rent natrium, mens på den andre elektroden er ren gassformig klor dannet.
Natriumkationen reduseres til katoden Na⁺ → na (l); Anionen klorid oksiderer anionen Cl⁻ → ½ Cl₂ (g).
Hva er metallnatrium for
Metallisk natrium brukes i Laboratorier av forskning for eksperimenter spesifikk, i metallurgi for utvinning av Titan (Ti) og også i noen reaktorer kjernefysisk som kjølemediumvæske. Et veldig lovende forskningsfelt angår batteriene til natrium. I dag er de vanligste batteriene de AL litiummen litium er et «Kritisk råstoff«, Så vi prøver å erstatte det med natrium, som er mye rikelig. Nylig har et team av forskere fra Korea Advanced Institute of Science and Technology utviklet en prototype Natriumbatteri som viste god ytelse.
Imidlertid har natriumbatterier noen ulemper Sammenlignet med litiumene. For eksempel har de en tetthet energi underordnetsom betyr at de transporterer mindre energi per vektenhet. For å gjøre en sammenligning har et typisk natriumbatteri en energitetthet på omtrent 160 WH/kg, mens et kommersielt litiumbatteri kan nå rundt 250 WH/kg. Dette innebærer mindre autonomi for natriumbatterier.
Til tross for dette er forskningen på natriumbatterier mye lovende. I fremtiden kan de representere et billigere og bærekraftig alternativ, spesielt i sektorer der den samme kraften som litiumbatterier ikke er nødvendig.

