En hjemmelaget te med den klassiske posen er et godt eksempel på løsningder vannet (løsningsmiddel) trekker ut forbindelsene som er til stede i bladene (oppløste). Dette skjer takket være en spontan prosess som heter spre, Som molekylene beveger seg fra områder der det er mer (med høy konsentrasjon, i posen) mot områder der det er mindre (med lav konsentrasjon, i vann) for å nå en balanse mellom de to områdene. Der Diffusjonshastighet Det avhenger også av temperatur: Den varme støyen, jo mer rister molekylene og beveger seg fra den ene siden til den andre ved å øke den kinetiske energien i systemet. Denne større agitasjonen akselererer utvinning av stoffer fra posen, for å få utgivelse av smaker, aromaer og farge. I kaldt vann, tvert imot, er prosessen mye tregere.
Te er en løsning
Når vi tilbereder te hjemme, er vi, fra et kjemisk synspunkt, forbereder en løsning. Dette begrepet indikerer en homogen blanding bestående av to komponenter: den løsningsmiddeli større mengde, og løsti mindre mengder og som er oppløst inne i løsningsmidlet.
I vår kopp te representerer vann løsningsmidlet, mens oppløste stoffer er alle molekylene som er til stede i de hakkede bladene som er inneholdt i posen: det er hovedsakelig Polyfenoler (spesielt katekiner), polysakkarider, alkaloider (som for eksempel Theinsom er strukturelt identisk med koffein) og saponiner. Når vi senker posen i vannet, begynner disse forbindelsene å vandre mot den omkringliggende væsken. Hastigheten som denne prosessen finner sted, avhenger av mange faktorer: en av de viktigste er temperatur vann.
Ved høyere temperaturer beveger molekylene seg mer
Der temperaturfra et mikroskopisk synspunkt, er ikke noe mer enn målet på Molekyler bevegelse: Jo mer varmt stoff, partiklene som komponerer det er raskere. Når vi snakker om bevegelse, mener vi molekylenes evne til å bevege seg til verdensrommet, å rotere og vibrere: alle disse bevegelsene bidrar til den så -kalt Kinetisk energisom vi kan forestille oss som en «bevegelsesenergi». Ved å øke temperaturen på et stoff øker også den kinetiske energien til molekylene.
Ved høye temperaturer beveger vannmolekyler seg med større intensitet: dette fenomenet, kjent i kjemi som Termisk agitasjonfører til en økning i den kinetiske energien i systemet. Vannmolekylene som beveger seg raskere De klarer å lettere dra de oppløste molekylene som er til stede i posen, Ved å spre dem raskere i væsken og øke spredningshastigheten som molekylene passerer fra posen til koppen vann. Resultatet? Fargen, smaken og aromaen av te sprer seg mye raskere enn hva som skjer i kaldt vann, Der molekylær bevegelse reduseres og ekstraksjonen av oppløste stoffer er tregere.
Hva er diffusjonen?
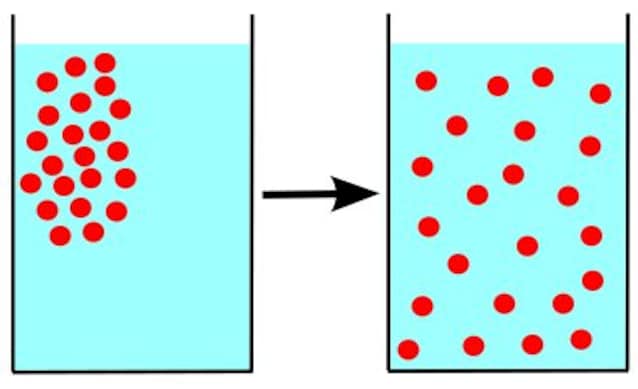
Passering av molekyler fra posen med vannte er en spontan prosess kalt «spre«: Forbindelsene beveger seg naturlig fra et høyt konsentrasjonsområde (bladene i posen) mot et lavt konsentrasjonsområde (vannet i koppen), til det når en situasjon med balansere.
Som ethvert fysisk fenomen kan diffusjonen også beskrives ved en matematisk lov: i dette tilfellet snakker vi om Første Fick Lawuttalt av den tyske fysikeren Adolf Fick i 1855. Den matematiske ligningen er som følger:
J = d Δc / Δx
- J representerer strømmen av molekyler som sprer seg (derfor det som kommer ut av posen) og representerer Diffusjonshastighet
- ΔC representerer Konsentrasjonsforskjell Mellom det første punktet og det endelige punktet, i vårt tilfelle det indre av posen og koppen vann
- Δx indikerer retningen som molekyler beveger seg, alltid i henhold til vårt eksempel, fra vannet til vannet.
- D kalles diffusjonskoeffisient, en parameter som avhenger av noen variable mengder som kjennetegner systemet, inkludert temperatur.
Denne formelen forklarer at hastigheten som molekylene passerer fra vannet til vannet er direkte proporsjonal med forskjellen i konsentrasjon og diffusjonskoeffisienten, derfor også til temperaturen.

