Smerte og nytelse har alltid vært ansett som motsatte opplevelser, men i virkeligheten er grensen mellom de to uskarp. Faktisk forteller moderne nevrovitenskap oss at i hjernen er skillet mellom de to mye mindre tydelig enn vi tror: de deler de samme kretsene, de samme nevrotransmitterne og påvirker hverandre direkte. Glede kan redusere smerte, kronisk smerte kan slå av evnen til å føle nytelse, og hjernen bruker en slags kontinuerlig balanse mellom de to for å veilede vår atferd.
Smerte og nytelse: to sider av samme sak
Smerte og nytelse. I årtusener har filosofer, poeter og religiøse mennesker beskrevet dem som absolutte motsetninger, de to ytterpunktene av menneskelig erfaring. Jeremy Bentham, en engelsk filosof fra det attende århundre, uttalte at alt menneskelig liv styres av disse to «suverene»: å flykte fra smerte og å søke nytelse. Likevel forteller moderne nevrovitenskap oss en mye mer spennende historie: i hjernen er ikke smerte og nytelse fjerne fiender, men naboer som deler de samme kretsene, de samme nevrotransmitterne og, i visse tilfeller, påvirker hverandre på overraskende måter. Glede er en midlertidig belønning, ofte forbundet med dopamin, mens smerte er en respons på negative stimuli.
Hjernen som arbiter av de to sensasjonene
Se for deg en idrettsutøver som midt i et avgjørende løp ikke kjenner smerten forårsaket av en forstuing. Eller tenk på den skarpe nytelsen av chilipepper eller et iskrembad. Hvorfor «slår» hjernen av smerte eller transformerer den til en positiv følelse under visse omstendigheter?
Svaret ligger i det forskerne kaller Motivasjons-beslutningsmodell, en modell foreslått av nevroforsker H. Fields. Den underliggende ideen er like enkel som den er elegant: Hjernen er hele tiden opptatt med å bestemme hva som er viktigst for å overleve. Hvis en mer presserende belønning eller trussel er i spill, kan smerten bli midlertidig undertrykt. I evolusjonære termer er det fornuftig: et dyr som flykter fra et rovdyr har ikke råd til å stoppe på grunn av et skrapet kne.
Denne smertedempende mekanismen formidles av et sofistikert synkende smertemoduleringssystem som starter fra hjernestammen og kommuniserer med prefrontal cortex, hypothalamus og amygdala. Og de viktigste kjemiske hovedpersonene i dette systemet er to: endogene opioider og den dopamin.
Rollen til endogene opioider og dopamin
Hjernen vår produserer stoffer, kalt endogene opioider (som f.eks endorfiner) og dopamin som frigjøres under både smertefulle og hyggelige opplevelser. Spesielt en struktur kalt nucleus accumbenset slags «lystsenter» i hjernen, spiller en nøkkelrolle i begge typer opplevelser.
- Endogene opioider (endorfiner): de modulerer den emosjonelle komponenten av smerte, hvor vondt det gjør, og forsterker det behagelige ved opplevelser. De eliminerer ikke det smertefulle signalet, men de gjør det mer utholdelig. De frigjøres både under smerte og under hyggelige opplevelser (mat, musikk, sex).
- Dopamin: det er ikke nevrotransmitteren av nytelse, men av motivasjonen til å søke den. Ved smerte har det smertestillende effekter og stimulerer frigjøringen av opioider.
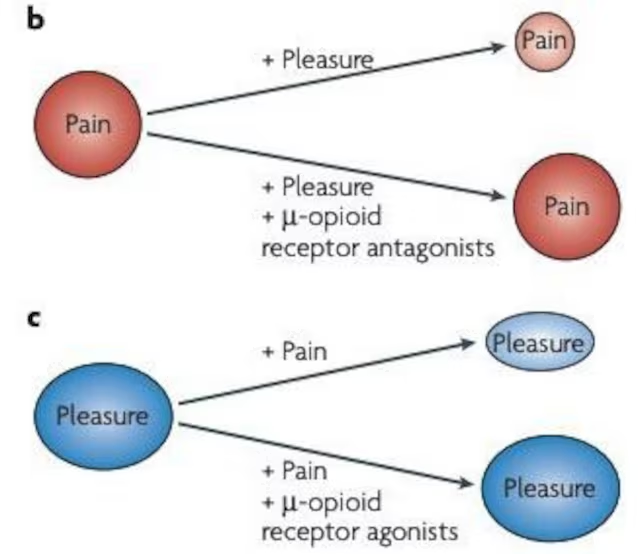
Smerte og nytelse: samme hjerneområder, to motsatte opplevelser
Det kanskje mest overraskende beviset gjelder nevroanatomi. Da forskerne kartla hjerneområdene aktivert av smertefulle og hyggelige opplevelser, fant de en slående overlapping. Den fremre cingulate cortex, insula, orbitofrontal cortex, amygdala, nucleus accumbens, thalamus, mellomhjernen: alle disse strukturene er aktive både under nytelse og smerte, om enn med forskjellige mønstre.
Spesielt interessant er tilfellet med den ventrale pallidum og nucleus accumbens: begge inneholder små områder, kalt «pleasure hot spots», der opioidstimulering øker behageligheten til en søt smak. Men de samme strukturene inneholder også populasjoner av nevroner som reagerer på smerte. Og plasseringen av disse to typene nevroner, i pallidum, er tilstøtende: «smertenevronene» er lokalisert lateralt for lystneuronene. En anatomisk nærhet som antyder kontinuerlige funksjonelle interaksjoner mellom de to systemene.